NCS - TUTORIA - 15/05/23 - SP 3.2
- thikow

- 15 de mai. de 2023
- 31 min de leitura
Atualizado: 24 de mai. de 2023
SP 3.2 - Motor envenenado
Problemas
· Palpitação durante atividades físicas
· Sedentarismo
· Tabagismo
· Má alimentação
· Pais hipertensos
· Hipercolesterolemia familiar
· Obesidade
· HAS
· Dislipidemia
· Placa de ateroma
· Comer coisas de origem animal
· Uso da Sinvastatina
Hipóteses
· O indivíduo está com angina devido a arteriosclerose
· Má alimentação, tabagismo e sedentarismo e obesidade predispõe para hipertensão
· Má alimentação, tabagismo e sedentarismo predispõe para obesidade
· Alimentação preferencialmente obtida através de origem animal, aumenta o colesterol e consequentemente a dislipidemia
· O histórico familiar dele predispõe ele ter doenças cardiovasculares
· O estresse pela doença da mãe alterou os hábitos alimentares do Antunes favorecendo a dislipidemia
· Hipercolesterolemia do paciente é de fundo genético (familiar/primaria) – Secundária é quando se alimenta mal.
Questões
1- O que são os lipídios, quais os principais tipos e funções?
2- Como e onde ocorre a digestão e absorção dos lipídeos? Descreva a digestão (enzimas e função da bile), absorção (onde acontece e como), principal saber sobre a absorção pelo NPC1L1 (cai na prova)?
3- Quais são as lipoproteínas e como e para onde elas fazem o transporte dos lipídeos?
4- O que é e como e onde acontece a lipólise? Betaoxidação
5- Como e onde acontece a lipogênese. Como a via das pentoses contribui para a lipogênese?
6- Como o colesterol é sintetizado? (HMG-CoA redutase – é uma estatina)
7- Como a sinvastatina funciona?
8- Quais as políticas publicas de prevenção de obesidade e hipertensão?
R1 - O que são os lipídios, quais os principais tipos e funções?
São classificados em dois grandes grupos quanto ao seu ponto de fusão:
• Gorduras – São glicerídeos de ácidos saturados. Gorduras de origem animal, que à temperatura ambiente se tornam sólidas.
• Óleos – São glicerídeos de ácidos insaturados. Gorduras de origem vegetal que não se tornam sólidas em temperatura ambiente.

· Cada grama de gordura gera 9 kcal, enquanto, cada grama de carboidratos ou proteínas geram 4 Kcal/g
· Fonte de ácidos graxos essenciais
· Maior reserva energética (não deve passar dos 30%
do V.C.T.)
· Armazenado nos adipócitos
Funções
· Reserva de energia e combustível celular
· Membranas celulares (fosfolipídios e glicolipídios)
· Isolamento e proteção de órgãos
· Impermeabilizante (ceras/ceramidas)
· Isolante térmico
· Hormonal (esteróides/colesterol)
· Anti-oxidante (Vitaminas A e E)
· Digestiva (sais biliares)
Esses compostos são formados, essencialmente, por átomos de hidrogênio, carbono e oxigênio, mas também podem conter fósforo, nitrogênio e enxofre.
O metabolismo energético dos lipídios acontece secundariamente ao dos carboidratos, o que torna os lipídios, que contém ácidos graxos, notadamente os triacilgliceróis (trigligerídeos), as principais biomoléculas de reserva energética. De fato, a própria absorção dos lipídeos se dá de forma a favorecer esta função.
Glicerídios – São lipídios que atuam como reserva energética e isolante térmico, além de amenizarem impactos mecânicos. Óleos e gorduras são exemplos de glicerídios e podem ser classificados de acordo com o seu ponto de fusão. Gorduras são lipídios sólidos, na temperatura ambiente, obtidos a partir de animais. Já os óleos são lipídios líquidos, na temperatura ambiente, obtidos a partir de produtos vegetais.
Ceras – Atuam como importantes substâncias impermeabilizantes. São comuns em folhas e frutos, mas também são produzidas por animais, como é o caso das aves e das abelhas.
Esteroides – Destacam-se por não possuírem ácidos graxos em sua estrutura, sendo bastante diferentes dos outros lipídios. Como exemplo de esteroides, podemos citar os hormônios sexuais e o colesterol. Sem dúvidas, o esteroide mais conhecido e mais importante é o colesterol, que, apesar de ser fundamental para o organismo, está bastante relacionado com problemas cardíacos.
Fosfolipídios – Lipídios que possuem fosfato em sua estrutura e são encontrados nas membranas celulares e no tecido nervoso.
Carotenoides – São importantes pigmentos fotossintetizantes que, além de participarem desse processo, dão coloração a frutos, flores e outras partes vegetais. A coloração gerada pelos carotenoides vai do amarelo ao vermelho.
R1 - ALTERNATIVA
Os lipídios se definem como biomoléculas insolúveis em água que podem ser extraídas das células por solventes orgânicos, como éter, clorofórmio, hexano, acetona, etc. Suas conformações e funções são muito variadas. Os lipídios mais abundantes são os triglicerídeos, que têm função armazenadora de energia; os fosfolipídios fazem parte das membranas biológicas; o colesterol tem importantes funções biológicas, sendo precursor dos hormônios esteroidais e dos ácidos biliares e também fazendo parte da estrutura das membranas; o ácido araquidônico é precursor de prostaglandinas, tromboxanos e leucotrienos, compostos que regulam vias metabólicas e processos inflamatórios. Finalmente, as vitaminas lipossolúveis têm importantes funções metabólicas.
Entre as principais funções dos lipídios no organismo estão as seguintes:
· Constituir a estrutura das membranas biológicas (fosfolipídios, colesterol)
· Manter reservas de energia (triglicerídeos)
· Fornecer moléculas precursoras dos hormônios esteroidais (colesterol) e das prostaglandinas (ácido araquidônico)
· Manter o calor corporal e servir de suporte e proteção das vísceras (triglicerídeos)
A função de servir como compostos armazenadores de energia é exercida pelos triglicerídeos de forma mais eficiente que os glicídios, devido a sua estrutura menos oxidada formada por cadeias hidrocarbonadas. Enquanto a oxidação total de um triglicerídeo rende aproximadamente 37,6 kJ/g, a oxidação de um glicídio rende 16,7 kJ/g. Por outro lado, por estarem menos hidratados do que os glicídios, os triglicerídeos podem ser armazenados de forma mais concentrada. Devido a sua hidrofobicidade e completa insolubilidade na água, os triglicerídeos ficam limitados no espaço das gotas citoplasmáticas que não afetam a osmolaridade do citosol e, portanto, não contêm água de solvatação como os glicídios, o que aumenta o peso e o volume da célula.
A própria insolubilidade dos triglicerídeos faz com que os processos de digestão e transporte desses compostos sejam mais complicados, pois eles devem ser emulsificados no intestino antes de serem absorvidos e somente podem ser transportados no sangue mediante as lipoproteínas.
Os lipídios podem ser classificados em:
· Lipídios compostos, aqueles que após hidrólise rendem ácidos graxos; entre eles estão: (a) triglicerídeos: compostos por glicerol e ácidos graxos; (b) fosfoglicerídeos: compostos por glicerol, ácidos graxos, grupos fosfato e grupos amino-álcool; (c) esfingolipídios: compostos por esfingosina, ácidos graxos e outros grupos (glicídios, grupos fosfato e amino-álcoois).
· Lipídios simples, aqueles que após hidrólise não produzem ácidos graxos; entre eles estão: (a) esteróis: o mais importante nos animais é o colesterol; (b) derivados de ácidos graxos com função metabólica, como as prostaglandinas; (c) isoprenoides: vitaminas lipossolúveis A, D, E e K.
Os ácidos graxos formam parte da estrutura da maioria dos lipídios. São ácidos orgânicos hidrocarbonados, altamente reduzidos, com cadeias de variado comprimento (entre 1 a 36 carbonos) e proporcionam aos lipídios seu caráter hidrofóbico. Os ácidos graxos mais abundantes nos animais são os de 16 e 18 carbonos.
Os ácidos graxos podem ter insaturações, ou seja duplas ligações, em suas cadeias. As insaturações geralmente estão depois do C-9 em direção ao grupo metilo-terminal (-CH3) sempre separadas por grupos metileno (…-CH=CH–CH2–CH=CH-…). Geralmente a dupla união tem configuração cis, o que ocasiona uma dobra rígida na estrutura do ácido. A dupla união é especificada com a letra grega delta maiúsculo (▲) e sua posição com um número sobrescrito. Os ácidos graxos existentes na natureza são maioritariamente de número par de átomos de carbono e são lineais, isto é, sem ramificações. A exceção está em alguns ácidos graxos bacterianos, que são ímpares e ramificados, como das bactérias do rúmen, cujos ácidos graxos são absorvidos no intestino e aparecem no leite dos ruminantes. O ponto de fusão do ácido graxo incrementa-se com o aumento do comprimento da cadeia, mas as insaturações diminuem o ponto de fusão em ácidos do mesmo número de carbonos.
Principais ácidos graxos e seus pontos de fusão
Ácido graxo Número de carbonos Ponto de fusão (°C)
Butírico 4 -4,3
Capróico 6 -2,0
Caprílico 8 16,5
Cáprico 10 31,4
Láurico 12 44,2
Mirístico 14 53,9
Palmítico 16:0 63,1
Palmitoléico 16:1 (▲9) -0,5
Esteárico 18:0 63,1
Oléico 18:1 (▲9) 13,4
Linoléico 18:2 (▲9,12) -5,0
Linolénico 18:3 (▲9,12,15) -11,0
Araquídico 20:0 76,5
Araquidônico 20:4 (▲5,8,11,14) -49,5
Lignocérico 24:0 86
Os ácidos graxos voláteis (AGV) são aqueles constituídos por 1 a 5 carbonos e devido a seu tamanho são hidrossolúveis. Têm importância em animais ruminantes, pois se acham em altas quantidades no rúmen, como produto da digestão dos glicídios. De especial importância no metabolismo energético destes animais são os ácidos acético, propiônico e butírico, bem como o derivado b-hidroxibutírico.
Ácidos graxos essenciais
A essencialidade, isto é, a necessidade de ingerir na dieta alguns ácidos graxos insaturados, particularmente o ácido linolénico, é conhecida desde 1928 quando Evans e Burr demonstraram a consequência da deficiência deste ácido em ratos. Os animais superiores não têm a capacidade metabólica de sintetizar esses ácidos, devendo, portanto, ser fornecidos na dieta. Existem diferenças nos requerimentos dos ácidos graxos essenciais, dependendo da espécie animal. Os ácidos linoleico, linolénico e araquidônico, adicionados na dieta corrigem os problemas ocasionados por sua deficiência, tais como eczemas e lesões no aparelho urinário. Os ácidos graxos essenciais encontram-se principalmente nos óleos vegetais; sua função é diversa e não muito bem definida, participando na síntese de prostaglandinas, substâncias com função hormonal e de leucotrienos, substâncias relacionadas com as células de defesa. Entretanto, sua principal função está relacionada com a integridade estrutural das membranas biológicas, como componentes dos fosfolipídios.
Triglicerídeos
Os triglicerídeos são os lipídios mais abundantes na natureza e estão conformados por glicerol e três ácidos graxos, unidos mediante ligação éster. São conhecidos também como gorduras neutras, já que não contêm cargas elétricas e nem grupos polares.
Os triglicerídeos conformam os depósitos gordurosos no tecido adiposo animal e nos vegetais, principalmente nas sementes, mas não fazem parte das membranas biológicas. A principal função dos triglicerídeos é servir como reserva de energia. Por ser compostos menos oxidados que os glicídios, as gorduras rendem maior quantidade de energia na oxidação celular; também, por sua característica hidrofóbica, as gorduras armazenam-se em menor espaço do que os glicídios, tendo capacidade praticamente ilimitada de armazenagem. Os glicídios, pelo contrário, por estarem hidratados têm um limite de armazenamento. A gordura animal armazena-se nos adipócitos do tecido graxo, embaixo da pele, na cavidade abdominal e na glândula mamária e além de servir de reserva energética, protege aos animais contra o frio na forma de isolante e protege também as vísceras amortecendo os movimentos fortes. A característica do triglicerídeo depende do tipo e proporção dos ácidos graxos que o conformam; nas plantas, a proporção de ácidos graxos insaturados C-16 e C-18 é maior que nas gorduras de origem animal; nos derivados lácteos, tem importância a presença de ácidos graxos de cadeia curta, os quais provêm do metabolismo ruminal; na gordura animal, a soma dos ácidos graxos saturados C-16 e C-18 é um pouco maior que a dos ácidos graxos insaturados. Os óleos de origem vegetal são geralmente líquidos na temperatura ambiente (22ºC), devido à maior proporção de ácidos graxos insaturados, enquanto que as gorduras de origem animal são sólidas nessa mesma temperatura, pela maior presença de ácidos graxos saturados. A manteiga tem ponto de fusão mais baixo (32°C) do que a gordura animal (59,6°C) devido à presença de ácidos graxos de cadeia curta.
Rancidez dos lipídios
Os lipídios podem sofrer rancidez hidrolítica quando existe liberação dos ácidos graxos unidos ao glicerol por causa de enzimas hidrolíticas, geralmente procedentes de microorganismos; o exemplo típico é o ácido butírico liberado da manteiga, que dá um cheiro característico. Os lipídios também podem sofrer rancidez oxidativa por oxidação dos carbonos comprometidos nas duplas ligações dos ácidos graxos insaturados, devido a um ambiente com alta concentração de O2 ou à presença de peróxidos ou radicais livres produzidos no metabolismo nas células. As membranas celulares são as mais afetadas com esta oxidação, já que altera a estrutura dos fosfolipídios e o próprio funcionamento da membrana. Para evitar esses eventos, a célula utiliza mecanismos de redução de peróxidos, através do glutation e da vitamina E. A teoria do envelhecimento assinala que este se apresenta quando os mecanismos antioxidantes começam a falhar. Os ácidos graxos oxidados dificilmente são absorvidos pelo intestino e podem causar disfunções intestinais. Também podem interferir com o metabolismo lipídico causando problemas como fígado gorduroso, ataxia e distrofia muscular.
Lipoproteínas
Após a sua absorção, na célula da mucosa intestinal, os triglicerídeos e fosfolipídios reesterificados se combinam com uma pequena fração de proteína para formar os quilomícrons, lipoproteínas de transporte dos lipídios desde o intestino até o fígado. Além desses lipídios, os quilomícrons também carregam ésteres de colesterol, colesterol livre, ácidos graxos livres e vitaminas lipossolúveis. O processo de formação dos quilomícrons depende da síntese da fração proteica pela mucosa intestinal. Nenhum dos lipídios encontrados no plasma pode circular livremente pela corrente sanguínea devido a sua insolubilidade em meio aquoso e para seu transporte têm de estar unidos a lipoproteínas plasmáticas específicas. Os ácidos graxos livres viajam pelo plasma associados à albumina. As lipoproteínas plasmáticas são proteínas associadas com lipídios que servem para transportar pelo sangue triglicerídeos e, em menor quantidade, fosfolipídios e colesterol. A separação de lipoproteínas mediante ultracentrifugação divide 6 frações em função de suas diferenças de densidade: HDL (lipoproteínas de alta densidade), LDL (lipoproteínas de baixa densidade), IDL (lipoproteínas de densidade intermediária), VLDL (lipoproteínas de densidade muito baixa), quilomícrons e remanentes de quilomícrons. As diferentes lipoproteínas diferem entre si conforme a proporção de lipídios que contém (entre 50 a 90%) o que causa diferente densidade; quanto maior for o conteúdo de lipídios, menor é a densidade da lipoproteína.
Composição percentual dos componentes das principais lipoproteínas plasmáticas
Lipoproteína Densidade (g/mL) Diâmetro (nm) Triglicerídeos Fosfolipídios Colesterol Proteína
Quilomícron 0,92-0,96 50-200 85 9 4 2
VLDL 0,95-1,006 28-70 60 18 15 10
LDL 1,01-1,063 20-25 10 22 45 25
HDL 1,07-1,21 8-11 3 30 18 50
As lipoproteínas com maior conteúdo de lipídios e também as de maior tamanho são os quilomícrons, sintetizadas nas células intestinais, estando encarregadas basicamente de transportar triglicerídeos desde o intestino delgado até o fígado. Os remanescentes de quilomícrons se referem a partículas derivadas dos quilomícrons após a remoção parcial de triglicerídeos pela ação da lipoproteína-lipase, enzima de membrana das células, sendo, portanto, ricos em colesterol e mais densos que os quilomícrons.
As VLDL transportam triglicerídeos do fígado para os tecidos periféricos e são sintetizadas no fígado. As LDL e IDL são geradas a partir de VLDL no plasma por ação da enzima lipoproteína-lipase. As LDL são as lipoproteínas que transportam maior quantidade de colesterol. As IDL, cuja densidade está entre 1,006 e 1,019 são designadas como importantes intermediários lipolíticos entre VLDL e LDL.
As HDL são produzidas no fígado e transportam fosfolipídios e ésteres de colesterol desde os tecidos periféricos até o fígado para sua excreção. As lipoproteínas HDL e LDL transportam cerca de 90% do colesterol e dos fosfolipídios no plasma. O colesterol plasmático no cão é transportado igualmente por LDL (colesterol-LDL) e por HDL (colesterol-HDL). Nos humanos, o colesterol é transportado maioritariamente por LDL, e cerca de 20% por HDL. Esta divisão é importante, porque o aumento de colesterol-LDL nos humanos tem sido associado com aterosclerose (acúmulo de gordura nas artérias) e, portanto, com o risco de sofrer problemas cardíacos, enquanto que o aumento de colesterol-HDL tem sido associado com diminuição do risco de sofrer problemas cardíacos.
As porções proteicas das lipoproteínas chamam-se apoproteínas das quais existem vários tipos e parecem influir na afinidade das lipoproteínas por certos receptores celulares, regulando a distribuição dos lipídios nos diferentes tecidos. As apoproteínas B, C e E estão associadas a VLDL. Na conversão de VLDL em IDL e LDL, se perdem algumas apoproteínas, de forma que a IDL contém apo B e E, ao passo que a LDL possui quase exclusivamente apo B. Por outro lado, a apoproteína mais importante na HDL é a apo C. A falha na síntese de apoproteínas no fígado, devido a intoxicações (clorofórmio, micotoxinas) ou devido a processos patológicos, leva à acumulação de lipídios no fígado causando fígado gorduroso ou lipidose hepática. Por outro lado, a deficiência de colina causa o mesmo problema devido à falta de fosfolipídios, necessários para a formação do complexo lipoproteico. A lipoproteína-lipase, enzima presente no endotélio dos capilares e na membrana das células adiposas, hidrolisa os triglicerídeos presentes nas lipoproteínas circulantes em ácidos graxos e glicerol, cumprindo um importante papel no equilíbrio das diferentes lipoproteínas. O glicerol permanece no sangue e volta para o fígado onde é metabolizado, enquanto que os ácidos graxos entram nas células mediante um transporte passivo facilitado. Dentro da célula adiposa, os ácidos graxos são reesterificados para serem armazenados como triglicerídeos; na célula mamária fazem parte da gordura do leite e nas demais células são oxidados para a obtenção de energia.
R2 - Como e onde ocorre a digestão e absorção dos lipídeos? Descreva a digestão (enzimas e função da bile), absorção (onde acontece e como), principal saber sobre a absorção pelo NPC1L1 (cai na prova)?
(Triacilglicerol/triglicérides/triglicerol são a mesma coisa com nomes diferentes – 3 ácidos graxos grudados em um glicerol)
Os lipídios são compostos orgânicos com grande valor energético, servindo como alimento para o organismo. De maneira geral, apresentam como características:
São lipossolúveis, ou seja, são insolúveis em água;
Solúveis em solventes orgânicos, tais como o éter e a acetona;
Estão presentes no metabolismo de vegetais e animais;
Todos contêm em sua estrutura átomos de carbono, hidrogênio e oxigênio e, alguns lipídios podem conter nitrogênio e fósforo;
Através da hidrólise produzem ácidos graxos, ou ainda, combinam com os ácidos graxos para formar ésteres.
Os lipídios podem ser adquiridos através da dieta, onde serão absorvidos no intestino, ou podem ser produzidos de forma endógena, ou seja, pelo próprio organismo.
Em determinadas situações, o tecido adiposo retira lipídios da circulação sanguínea e os armazena na forma de gordura, os triacilgliceróis, para serem utilizados como fonte de energia. Assim, quando necessário, os triacilgliceróis são hidrolisados, formando glicerol e ácidos graxos, que caem na corrente sanguínea e são utilizados pelos tecidos, como o fígado e os músculos. O fígado é o principal sintetizador de lipídios endógenos.
Para que possam ser absorvidos, os lipídios precisam sofrer a digestão. Os lipídios provenientes da dieta estimulam a secreção de enzimas presentes em glândulas situadas na base da língua, conhecidas como lipase lingual. Contudo, não ocorre a hidrólise dos lipídios na boca, que são dirigidos até o estômago. Uma vez no estômago, a lipase gástrica promove a continuidade do processo, contudo, o pH altamente ácido dificulta a ação enzimática, onde a maior parcela da digestão acontece no intestino delgado. Uma vez no duodeno, o bolo alimentar com o pH ácido acaba por induzir a liberação do hormônio digestivo colecistocinina (CCK), também conhecido como pancreozimina. O CCK faz com que a vesícula biliar sofra contração e liberação da bile para o duodeno, também estimulando a secreção pancreática. Os lipídios são emulsificados pela ação dos sais biliares, formando micelas mistas de triacilgliceróis, que sofrem a digestão pela ação da lipase pancreática, liberando ácidos graxos. Desta forma, os ácidos graxos podem ser absorvidos pelas células que compõem o intestino, os enterócitos, e reconvertidos em triacilgliceróis, onde juntamente com o colesterol e apoliproteínas, irão formar o quilomícron. Os quilomícrons (QM) são então secretados nos vasos linfáticos e corrente sanguínea, sofrendo ação de lipases lipoprotéicas e gerando ácidos graxos e glicerol. Esses ácidos graxos serão oxidados e utilizados como fonte de energia, ou formar ésteres, para serem armazenados nos adipócitos ou células musculares, principalmente.
No fígado, os triacilgliceróis que compõem os QM são reagrupados, sendo enriquecidos por proteínas, ocorrendo a síntese da lipoproteína de densidade muito baixa (VLDL), que contém entre 80 a 90% de lipídios. O VLDL também sofrerá hidrólise pela lipase lipoprotéica, promovendo a liberação de ácidos graxos. Ao sair do fígado, o VLDL terá como objetivo levar triglicérides para os tecidos e, ao absorver os triglicérides, acaba por aumentar sua densidade, resultando na LDL. Assim, os QM que são reagrupados também podem formar:
LDL (low density lipoprotein): lipoproteína de baixa densidade, contendo aproximadamente 70% de lipídios.
HDL (high density lipoprotein): lipoproteína de alta densidade, com 45% de lipídios.
Podemos concluir que o tamanho da lipoproteína está diretamente relacionado à quantidade de proteína e lipídio que as compõem, sendo que a VLDL é a que possui mais lipídios e menor concentração de proteínas. O HDL acaba por apresentar mais proteínas e menor quantidade de lipídios.
A função do LDL está em transportar triglicérides para os tecidos. Por esta razão, é designado como o mau colesterol. O HDL promove nos tecidos a troca do colesterol por triglicérides, transportando-os de volta ao fígado, onde será metabolizado. Também, capta o colesterol dos quilomícrons, que é excretado na forma de sais biliares. Devido à esta ação, é tido como o bom colesterol. Para a adequada saúde, deve-se manter bons níveis de lipídios circulantes.
PROTEÍNA NPC1L1
A NPC1L1 é uma proteína politópica que consiste em treze domínios transmembranares. Cinco desses domínios detectam esteróis (SSD). O SSD também é encontrado em outras proteínas transmembranares, todas envolvidas no metabolismo do colesterol. A ligação do colesterol é feita no domínio N terminal da NPC1L1, resultando na entrada do colesterol.
Diversos estudos demonstraram que o transporte de colesterol dependente da NPC1L1 pode ser regulado pela endocitose mediada por clatrina. Em estado estacionário, as proteínas NPC1L1 são encontradas principalmente no compartimento de reciclagem endocítica (ERC). Quando há depleção do colesterol, as proteínas NPC1L1 se movem do ERC para a membrana plasmática. Se houver repleção de colesterol, este será detectado pela NPC1L1 e incorporado à membrana plasmática. Posteriormente, ele é internalizado e movido para o ERC. A NPC1L1 é amplamente expressa nos tecidos humanos e está presente principalmente no fígado e no intestino delgado.
NPC1L1 INTESTINAL
A NPC1L1 é amplamente expressa no jejuno e íleo proximal e está localizada especificamente na membrana dos enterócitos intestinais, onde ocorre a absorção do colesterol. Ratos deficientes em NPC1L1 apresentam redução de 70% da absorção intestinal de colesterol, dessa forma, atenuam a hipercolesterolemia induzida pela dieta. O colesterol é transportado para dentro das células pela NPC1L1. Diversos estudos demonstraram que a NPC1L1 tem especificidade pela absorção de esteróis. Os esteróis estão significativamente reduzidos em ratos deficientes em NPC1L1 ou tratados com ezetimiba. A recaptação de fitosteróis também é dependente da NPC1L1, porém a NPC1L1 tem maior afinidade pelo colesterol do que pelos fitosteróis.
NPC1L1 HEPÁTICA
Em humanos, há ampla expressão de NPC1L1 no fígado. O fígado é o principal local em que ocorre a homeostase do colesterol. Nele, há biossíntese de colesterol pela HMG-CoA redutase, liberação de lipoproteínas, armazenamento por esterificação, degradação e a conversão em ácido biliar para a remoção do colesterol, e regulação da absorção intestinal de lípides.
Comparado ao conhecimento sobre a NPC1L1 intestinal, as funções da NPC1L1 hepática ainda são em grande parte desconhecidas. Estudos com ratos que receberam NPC1L1 hepática humana revelaram redução do colesterol no ácido biliar e aumento do colesterol hepático. A ezetimiba diminuiu o colesterol biliar em pacientes com litíase biliar e em ratos. Essas observações sugerem que a NPC1L1 pode contrabalançar a secreção biliar de colesterol, evitando a perda de colesterol no transporte para os hepatócitos.
FITOESTEROL
Fitoesteróis competem nesse receptor com o colesterol, então uma abordagem que pode ser realizada é a prescrição de fitoesteróis.
INIBIDOR DA NPC1L1: EZETIMIBA
A ezetimiba é o primeiro fármaco de uma nova classe de inibidores seletivos da absorção de colesterol. Ela é absorvida e metabolizada pelo intestino e pelo fígado para seu glicuronídeo. A ezetimiba e seu metabólito inibem a absorção intestinal de colesterol por impedir o transporte de colesterol da luz intestinal para dentro dos enterócitos do intestino delgado, resultando em redução de 15% a 20% do colesterol plasmático.
No fígado, a ezetimiba diminui a entrega de colesterol, com consequente aumento da retirada de colesterol da circulação para os hepatócitos, através da regulação pelo receptor de LDL.
Clinicamente foi comprovada a eficácia da ezetimiba no tratamento da hipercolesterolemia. Por muito tempo, a molécula-alvo da ezetimiba não foi identificada. A ezetimiba impede a ligação específica da NPC1L1 e a internalização do colesterol, o que resulta em inibição da recaptação de colesterol no fígado, mediada pela NPC1L1. Com esses dados, foi demonstrado que a NPC1L1 é um alvo molecular direto da ezetimiba.
NPC1L1 E DOENÇAS
Existe forte relação entre níveis elevados de colesterol e a incidência de aterosclerose. O tratamento com ezetimiba e a deleção da NPC1L1 diminuem significativamente a absorção de colesterol e os níveis plasmáticos de colesterol; com isso, observa-se a inibição do desenvolvimento de aterosclerose. A ezetimiba diminui significativamente os níveis de LDL-colesterol em indivíduos com hipercolesterolemia. Ela também melhora a síndrome metabólica e a esteatose hepática não alcoólica e, devido à forte correlação entre a esteatose hepática não alcoólica e a resistência à insulina, constatou-se que a ezetimiba é capaz de promover a redução da resistência à insulina, com melhora da hiperglicemia, que por sua vez ocorre pelo aumento do tamanho pancreático e da massa de células beta, pelo aumento do peptídeo-1 semelhante ao glucagon (GLP-1) e pela redução da atividade da dipeptidil peptidase-4 (DPP4) sérica.
R3 - Quais são as lipoproteínas e como e para onde elas fazem o transporte dos lipídeos?
LIPOPROTEÍNAS
Os lipídeos e as proteínas associam-se de forma não covalente formando lipoproteínas, cuja função é a de transportar triacilgliceróis e colesterol no plasma sanguíneo.
Estrutura das lipoproteínas
Os fosfolipídeos, os triacilgliceróis e o colesterol são muito pouco solúveis em solução aquosa. Por essa razão, eles são transportados pela circulação como componentes de lipopro- teínas, que são partículas globulares semelhantes a micelas consistindo em um núcleo apoiar de triacilgliceróis e de ésteres de colesteril envolto por um revestimento anfifílico de proteínas, fosfolipídeos e colesterol. As lipoproteínas são classificadas em cinco categorias, com base em suas propriedades físicas e funcionais:
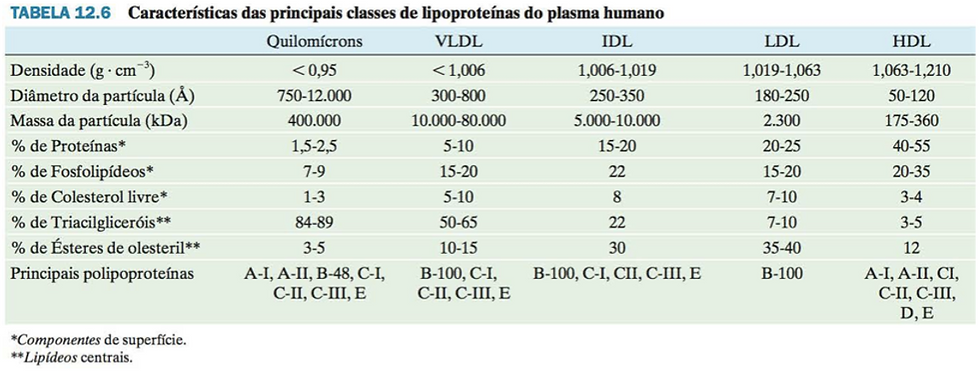
1. Quilomícrons, que transportam colesterol e triacilgliceróis exógenos (de origem externa, ou seja, da dieta) do intestino para os tecidos.
2-4. Lipoproteínas de muito baixa densidade (VLDLs, de very low density lipoproteins), lipoproteínas de densidade intermediária (IDLs, de intermidiate density lipopro- teins) e lipoproteínas de baixa densidade (LDLs, de low density lipoproteins) constituem um grupo de partículas relacionadas que transportam colesterol e triacilgliceróis endógenos (produzidos internamente) do fígado para os tecidos (o fígado sintetiza triacilgliceróis a partir do excesso de carboidratos; Seção 25.4).
5. Lipoproteínas de alta densidade (HDLs, de high density lipoproteins), que transportam colesterol endógeno dos tecidos para o fígado.
Os quilomícrons perdem os lipídeos nos capilares dos tecidos periféricos
Os quilomícrons, que são formados na mucosa intestinal, têm a função de manter o colesterol e os triacilgliceróis exógenos em solução aquosa. Essas lipoproteínas são liberadas na linfa intestinal (conhecida como quilo), que circula pelos vasos linfáticos até ser drenada pelo ducto torácico para as grandes veias do corpo. O quilo, normalmente transparente, adquire uma aparência leitosa após uma refeição rica em gordura.
Os quilomícrons aderem a sítios de ligação na superfície interna (endotélio) dos capilares nos músculos esqueléticos e no tecido adiposo. Nesses locais, alguns minutos após terem entrado na corrente sanguínea, seus triacilgliceróis são hidrolisados pela ação da lipase lipoproteica (LPL), uma enzima extracelular ativada pela apoC-11. Os monoacilgliceróis liberados e os ácidos graxos resultantes da hidrólise são captados pelos tecidos. Os quilomícrons diminuem de tamanho à medida que seus triacilgliceróis são gradativamente hidrolisados, até serem reduzidos a remanescentes de quilomícrons enriquecidos em colesterol. Esses dissociam-se do endotélio capilar e novamente entram na circulação, sendo captados pelo fígado. Os quilomícrons, portanto, transferem triacilgliceróis da dieta aos tecidos muscular e adiposo, e o colesterol da dieta para o fígado
Resposta AULA - A lipoproteína Quilomícron transporta em maior quantidade triglicerídeos do que colesterol. Lipase lipoproteica age sobre uma lipoproteína, ou seja, sobre o quilomícron, digerindo o triglicerídeo em ácidos graxos e glicerol, eles vão ser utilizados pelos músculos para gerar energia. O Quilomicron vai ser refeito para ser armazenado no tecido adiposo, sobra o quilomícron remanescente. Esse Quilomicron remanescente vai para o fígado. O fígado vai quebrar esse quilomícron, juntar ao colesterol e formar o VLDL. Tudo que aconteceu foi via exógena, a partir do momento que ele gera o VLDL vai para via endógena. Agora na via endógena a VLDL vai sair do fígado, tem mais proporcionalmente mais triglicerídeo do que colesterol. As lipoproteínas vão degradando esse VLDL no músculo, onde a lipase lipoproteica vai digerir esse triglicerídeo em acido graxo e glicerol. Esse material vai servir de energia e irá formar o IDL. Depois que tirar ainda mais triglicerídeos pela lipase lipoprotéica do IDL ele vira LDL.
LDL desta forma vai carregar mais colesterol. Colesterol é mais denso pois a lipoproteína é mais densa e vai sobrando colesterol e lipoproteína. LDL é a lipoproteína que vai carregar e fornecer o colesterol aos tecidos. Com aumento de LDL forma placa de ateroma. É uma das principais causas da hipercolesterolemia familiar é a mutação do receptor de VLDL
As VLDLs são degradadas como os quilomícrons
As lipoproteínas de densidade muito baixa (VLDLs), que são sintetizadas no fígado e têm função de transportar lipídeos, também são degradadas pela lipase lipoproteica (Fig. 12.86, à direita). Os remanescentes de VLDL aparecem na circulação, primeiro como IDL e depois como LDL. Na transformação da VLDL em LDL, todas as proteínas, com
exceção da apoB-100, são removidas e a maior parte do colesterol é esterificada pela enzima lecitina-colesterol-acil-transferase (LCAT), associada à HDL, como será discutido mais adiante. Essa enzima transfere um resíduo de ácido graxo do carbono 2 da lecitina para o colesterol, com a formação concomitante de lisolecitina (Fig. 12.87).
A HDL transporta colesterol dos tecidos para o fígado
A HDL desempenha essencialmente a função oposta à da LDL: remove o colesterol dos tecidos. A HDL é formada no plasma a partir de componentes obtidos, na sua maioria, da degradação de outras lipoproteínas. A HDL circulante provavelmente adquire seu colesterol extraindo-o das membranas plasmáticas, e converte-o em ésteres de colesteril pela ação da LCAT, uma enzima ativada pela apoA-1. A HDL funciona
portanto como um garimpeiro de colesterol.
O fígado é o único órgão capaz de eliminar quantidades
significativas de colesterol (pela conversão em ácidos biliares; Seção 25.6C). Isso ocorre pela atuação do RLDL e de um receptor específico para HDL, chamado SR-BI (de scavenger receptor classB type I). Metade da VLDL, após ter sido de- gradada a IDL e LDL, é captada pelo fígado pela endocitose mediada por receptor (Fig. 12.86, à direita). Os hepatócitos (as células do fígado), contudo, captam ésteres de colesteril da HDL por um mecanismo completamente diferente: a HDL ligada ao SR-BI transfere seletivamente os seus ésteres de colesteril para a célula. A HDL sem lipídeos então dissocia-se da célula e retorna à circulação.
a. Deficiência de receptores de LDL resulta em aterosclerose
O desenvolvimento da aterosclerose está fortemente correlacionado com o nível de colesterol plasmático. Isso é particularmente evidente em indivíduos com hipercolesterolemia familiar (HF). Os indivíduos homozigotos para essa doença têm níveis tão altos de LDL, rica em colesterol (o que é frequentemente referida como colesterol "mau"), em seu plasma que chegam a apresentar valores plasmáticos de colesterol de três a cinco vezes maiores do que o nível médio e 175 mg · 100 mL - • Essa situação resulta em deposição de colesterol na pele e nos tendões, sob a forma de nódulos amarelos, conhecidos como xantomas. Contudo, nos homozigotos, dano muito maior é causado pela formação rápida de ateromas, que podem causar morte precoce por infarto do miocárdio aos 5 anos. Os heterozigotos, que compreendem 1 pessoa em 500, são afetados menos severamente, desenvolvendo sintomas de doença das artérias coronárias após os 30 anos.
Células isoladas de indivíduos homozigotos para HF são totalmente desprovidas de RLDL funcional, enquanto as obtidas de heterozigotos possuem a metade da quantidade normal desses receptores. Por isso, os homozigotos, e em menor proporção os heterozigotos, são incapazes de utilizar o colesterol das LDLs. Suas células devem sintetizar a maior parte do colesterol que necessitam. Os altos níveis de LDL plasmático nesses indivíduos é o resultado de duas causas relacionadas:
1. Taxa de degradação reduzida devido à falta do RLDL. 2. Taxa de síntese aumentada a partir de IDL devido à incapacidade do RLDL em captar IDL.
Foram descobertas mais de 1.000 mutações no RLDL que causam HF. Esses mutantes foram agrupados em cinco classes dependendo da natureza do defeito que causam no funcionamento do RLDL (Fig. 12.91): (1) falha na produção de quantidades detectáveis de proteína; (2) falha parcial ou total no transporte para a membrana plasmática; (3) redução na interação com o ligante; (4) falha no direcionamento para as cavidades revestidas por clatrina e na internalização; e (5) defeitos na liberação e na reciclagem do ligante. Os mutantes da classe 4 são causados por mudanças nas assim chamadas sequências de classificação do RLDL, NPXR, no seu domínio citoplasmático, que se liga à AP2 nas cavidades revesti-
das por clatrina.
R4 - O que é e como e onde acontece a lipólise? Betaoxidação
Lipólise é um processo pelo qual há a degradação de lipídios em ácidos graxos e glicerol. Ocorre no tecido adiposo.
LIPÓLISE E β-OXIDAÇÃO DE ÁCIDOS GRAXOS
· β-oxidação = oxidação dos ácidos graxos para a obtenção de energia. Principal objetivo é produção de energia.
· Lipólise é exclusivamente catabólica (obtenção de energia), já a glicólise tinha fins catabólicos e anabólicos (com o uso de resíduos do ciclo de Krebs sendo desviados para anabolismo).
· Estimulados por glucagon (hepatócito e adipócito) e adrenalina (músculo esquelético e cardíaco).
· Sempre associadas ao jejum e atividade física.
· Nem todos os órgãos são capazes de usar ácidos graxos como fonte de nutrientes devido a sua baixa solubilidade (ex: cérebro).
· Os ácidos graxos também funcionam como detergentes.
· O fígado abastece os tecidos que não podem utilizar ácidos graxos com o produto da β-oxidação que são os corpos cetônicos.
· A β-oxidação é a via metabólica que segue a lipólise (mobilização de lipídios depositados nos adipócitos).
· Os lipídios da nossa dieta são preferenciais para tecido muscular e adiposo (são depositados através dos quilomicrons nesses tecidos).
Fígado
O fígado regula o que for remanescente da deposição de lipídio provenientes da nossa
dieta. Os quilomicrons captados pelo fígado vão ser remontados e laçados na circulação sanguínea na forma de VLDL (lipoproteína de muito baixa densidade). O fígado, portanto, trabalho nesse primeiro momento com a redistribuição dos triglicerídeos de maneira que haja utilização muscular, dependendo da necessidade, e principalmente estocagem na forma de tecido adiposo.
Participação principal na β-oxidação em situações catabólicas, principalmente a partir dos triglicerídeos que já estavam mobilizados no tecido adiposo e que por ação da adrenalina (atividade física) ou glucagon (jejum), fossem direcionados para o fígado.
Adipócito
Armazena em forma de gotas de triglicerídeos em vacúolo lipídico, sendo, portanto, o responsável por grande parte do volume das células, chegando a empurrar organelas. Essa gota de gordura não é somente formada por gordura, ela possui uma estrutura de semelhante à de uma micela, contudo, mais especializada por conter perilipina (proteína) agindo como interface entre o triglicerídeo na gota de gordura e o meio aquoso no citosol do adipócito.
A perilipina tem efeito estrutural e regulatório (pode ser fosforilada por PKA).
· Estímulo hormonal
· Receptor se liga ao glucagon ou adrenalina
· Ativação da proteína G
· geração de AMPc a partir da ativação da adenil-ciclase
· desencadeando a cascata de PKA
· fosforilando uma série de proteínas, dentre elas: Perilipina e lípase
Bibliografia:
Nelson, David L.; COX, Michael M. Princípios de bioquímica de Lehninger. Porto Alegre: Artmed, 2011. 6. ed. Porto Alegre: Artmed, 2014.
Lipogênese anabolismo/Lipólise catabolismo
A bile vai emulsificar essa gordura para que ela possa ser quebrada mais facilmente através da lipase presente no pâncreas e estomago, que irá quebrar a gordura em micelas, unidades menores mais fáceis de serem absorvidas
1- Durante o vídeo anote:
A- Níveis considerados normais de triglicérides, colesterol total e suas frações em jejum de 8 a 12 horas.
R- Triglicérides – Quando acima do valor limite representa o aumento do risco de doença cardiovascular progressivamente (quanto mais alto o nível, maior o risco)
Os valores normais de triglicerídeos são:
Até 150 mg/dL: normal.
Entre 150 e 199 mg/dL: limítrofe.
Entre 200 e 500 mg/dL: elevado.
Maior que 500 mg/dL: muito elevado.
Colesterol total – É a soma do HDL, LDL e do VLDL. Ter o colesterol total alto representa um risco elevado de doenças cardiovasculares.
Até 190 mg/dL
Frações – Como se trata de uma substância gordurosa, o colesterol não se dissolve no sangue, da mesma forma que gotas de óleo não se dissolvem na água. Portanto, para viajar através da corrente sanguínea e alcançar os tecidos periféricos, o colesterol precisa de um transportador. Essa função cabe às lipoproteínas produzidas no fígado. As principais lipoproteínas são:
VLDL (Very low-density lipoprotein).
LDL (Low-density lipoprotein).
HDL (High-density lipoprotein).
O LDL transporta colesterol e um pouco de triglicerídeos do sangue para os tecidos. O VLDL transporta triglicerídeos e um pouco de colesterol. Já o HDL é um transportador diferente, ele faz o caminho inverso, tira colesterol dos tecidos e devolve para o fígado que vai excretá-lo nos intestinos.
Portanto, enquanto o LDL e o VLDL levam colesterol para as células e facilitam a deposição de gordura nos vasos, o HDL faz o inverso, promove a retirada do excesso, inclusive das placas arteriais. Por isso, denominamos o HDL como “colesterol bom” e o VLDL e o LDL como “colesterol ruim“.
O colesterol derivado de gorduras saturadas e gordura trans favorece a produção de LDL, enquanto o consumo de gorduras insaturadas, encontrada no azeite, peixes e amêndoas, por exemplo, promovem a produção do HDL.
Portanto, ao dosarmos os valores das lipoproteínas transportadoras LDL, VLDL e HDL temos uma avaliação indireta da quantidade e da qualidade do colesterol que circula em nosso sangue. Por isso, o lipidograma, exame usado para dosar as lipoproteínas, é usado para avaliar os níveis de colesterol sanguíneos.
R5 - Como e onde acontece a lipogênese. Como a via das pentoses contribui para a lipogênese?
Ocorre no fígado, rim, cérebro, pulmão, glândula mamária e tecido adiposo.

A síntese ocorre no citossol, para onde deve ser transportado o acetil-CoA formado na mitocôndria a partir de piruvato. Mas como a membrana interna da mitocôndria é impermeável a acetil-CoA, ele se “transforma” em citrato (acetil-CoA + oxaloacetato gerando citrato pela enzima citrato sintase) que passa pela membrana, e fora desta é clivado na presença de ATP em oxaloacetato e acetil-CoA pela enzima citrato liase.
O oxaloacetato se transformará em fosfoenolpiruvato e depois para piruvato.
Acetil-CoA sofre uma carboxilação formando malonil-CoA pela enzima acetil-CoA carboxilase. Essa reação requer ATP e bicarbonato como fonte de CO2. Na 1a etapa o CO2 é ligado a um resíduo de biotina da enzima, usando energia derivada da hidrolise de ATP, o CO2 então é transferido para acetil-CoA.
O malonil-CoA se liga a outra Acetil-CoA e depois da saída de 1 CO2, gasto de 1 NADPH2 saída de água e gasto de1 NADPH2 ela será aumentada por 1 por malonil-CoA.
No total, a síntese de ácido palmítico (16 C) requer 1 acetil-CoA + 7 malonil-CoA, 14 NADPH2 E 7 voltas no ciclo de síntese.
Síntese de ácidos graxos e triglicérides, que serão armazenados no tecido adiposo.
Na hiperglicemia a insulina ativa as vias hipoglicemiantes que são a glicolise, glicogenese e via das pentoses.
· No caso do excesso de ATP, tanto ciclo de Krebs e cadeia respiratória são bloqueados causando o acúmulo de acetil-CoA dentro da mitocôndria, então o mesmo sai para o citoplasma na forma de citrato e através da enzima citrato liase no citoplasma celular volta a ser acetil- coA.
· Via citoplasmática, anaeróbica sendo sua molécula precursora o acetil- coA proveniente, por exemplo, do metabolismo de carboidrato, é uma via hipoglicemiante.
· Via síntese de acido graxo tem como hormônio ativador a insulina e como inibitório o glucagon.
· Via síntese de acido graxo ocorre nos tecidos hepáticos e principalmente no tecido adiposo.
· Enzima marca passo é a acetil-coA carboxilase ativada pela insulina e inibida pelo glucagon
· Biotina é uma vitamina que carrega o CO2 agindo juntamente a acetil- coA carboxilase na transformação do acetil-coA em malonil CoA que alonga a cadeia carbônica.
· Os ácidos graxos sintetizados aqui se combinam por esterificação com o glicerol com a finalidade de se produzir triglicérides armazenáveis usando a gliceroquinase (ativa no fígado e não no tecido adiposo) que transforma o glicerol em glicerofosfato, e glicerodesidrogenase que transforma a fosfodihidroxicetona em glicerofosfato.
· No tecido hepático a síntese de triglicérides ocorre por meio da enzima gliceroquinase que é abundante neste tecido, aqui as vias ativadas para a produção de gordura são:
- Via glicolítica
- Via das pentoses
- Via síntese de acido graxo
- Via síntese de triglicérides
- Glicogenese
· No tecido adiposo a síntese de triglicérides não ocorre por meio da enzima gliceroquinase que não existe neste tecido, então o glicerol fosfato é obtido através da fosfodiidroxicetona (via glicolítica ou pentoses).
- Via glicolítica
- Via das pentoses
- Via síntese de acido graxo
- Via síntese de triglicérides
VIA DAS PENTOSES
· Via das pentoses também denominada de desvio da hexose-monofosfato é uma importante via anaeróbica alternativa da utilização da glicose.
· Essa via não é produtora de ATP, mas sim de NADPH. via é reguladora da glicemia.
· Essa via exerce duas funções básicas:
-Produção de pentoses para a biosintese de nucleotídeos. (D-ribose)
-Produção de NADPH, agente redutor utilizado para biosintese de ácidos graxos e esteróides (colesterol e seus derivados), bem como para a manutenção da integridade das membranas dos eritrócitos.
· A via das pentoses é uma via citoplasmática, anaeróbica ocorrendo no fígado, glândulas mamarias, tecido adiposo e nas hemácias.
· Ocorre em duas etapas: fase oxidativa onde ocorre a produção de pentoses e fase não oxidativa onde ocorre a inter-converção de pentoses intermediários da via glicolítica.

A primeira reação da via das pentose fosfasto é a desidrogenação enzimatica da glicose-6-fosfato pela glicose-6-fosfato desidrogenase, para formar 6- fosfoglicono-d -lactona, que é hidrolizado para a forma ácida livre 6- fosfogliconato por uma lactonase especifica, sendo que o NADP+ é o receptor de elétrons No passo seguinte, o 6-fosfogliconato sofre desidrogenação e descarboxilacao pela 6-fosfogliconato desidrogenase para formar a D-ribulose- 5-fosfato, uma reação que gera a segunda molécula de NADPH2. A fosfopentose isomerase converte então a ribose-5-fosfato em D-ribose-5- fosfato. Em alguns tecidos, a via das pentoses fosfato termina neste ponto e a equação final pode ser escrita:
Glicose-6-fosfato + 2 NADP+ + H2O -------- ribose-5-fosfato + CO2 + 2 NADPH + 2 H+
O resultado líquido é a produção de NADPH2 para as reações de redução biossintetica e a produção de ribose-5-fosfato como precursora para a síntese de nucleotideos.
Proveniente desta mesma via poderemos destacar a síntese de D- glicuronato, importante na detoxificacao e na excreção de compostos orgânicos estranhos, e a formação de acido ascórbico ou vitamina C em seres que não.
Quando as pentoses não são usadas elas irão se combinar e voltar à via glicolítica usando as enzimas transaldolase e transacetilase:

Caso a pessoa tenha deficiência da enzima marca passo G6PD, terá um tipo de anemia hemolítica pois a glutationa é um potente agente antioxidante, e no interior da hemácias pode-se notar que há grande quantidade de oxigênio (potente oxidante), que retira elétrons da membrana dos eritrócitos, estourando-os.

A deficiência de desidrogenase de glicose-6-fosfato não exibir sinais e sintomas até que seus glóbulos vermelhos são expostos a determinadas substâncias químicas em alimentos, medicamentos, infecções ou stress. Em casos mais graves, a conseqüência mais importante da deficiência de G6PD é a anemia hemolítica. Os principais sintomas da anemia hemolítica são icterícia, urina escura, dor abdominal, dor nas costas, diminuição da contagem de células vermelhas do sangue, e bilirrubina elevada.
Os sintomas de deficiência de G6PD são mais comuns incluem:
*palidez (a palidez de pele mais escura as crianças às vezes é melhor visto na boca, especialmente nos lábios ou na língua) *cansaço extremo *batimentos rápidos do coração
*respiração rápida ou dificuldade em respirar *icterícia ou amarelamento da pele e dos olhos, especialmente em recém- nascidos *aumento do baço *urina escura, a cor do chá
Os recém-nascidos com deficiência de G6PD são cerca de 1,5 vezes mais chances de obter a icterícia neonatal do recém-nascido sem deficiência de G6PD. Uma vez que o gatilho é removido ou resolvidas, os sintomas de deficiência de G6PD geralmente desaparecem rapidamente, geralmente dentro de algumas semanas.
Resposta AULA
Piruvato é convertido em Acetil-CoA, que vai ser a base pra formação de lipídeos na glicogênese. Excesso de Acetil-CoA vai ser convertido em gordura, pois ele será deslocado para produção de lipídeos. Glicose ou lipídeos pode virar lipídeos.
R6 - Como o colesterol é sintetizado? (HMG-CoA redutase – é uma estatina)
O colesterol é um constituinte vital das membranas celulares e um precursor dos hormônios esteroides e dos ácidos biliares. Apesar de ser essencial à vida, sua deposição nas artérias está associada a doenças cardiovasculares e a derrames, duas das principais causas de mortalidade em seres humanos. Em um organismo saudável, um equilíbrio intrincado é mantido entre a biossíntese, a utilização e o transporte de colesterol, fazendo com que sua deposição prejudicial permaneça em um nível mínimo. Nesta seção, serão estudadas as rotas de biossíntese e de transporte de colesterol e de que modo elas são controladas. Será examinado também como o colesterol é utilizado na biossíntese de hormônios esteroides e de ácidos biliares.
A. Biossíntese do colesterol
Todos os átomos de carbono do colesterol são derivados do acetato. Observações sobre o padrão de incorporação levaram Konrad Bloch a propor que o acetato é primeiramente convertido em unidades isopropeno, unidades C5 que possuem o esqueleto de carbono de isopreno:
As unidades de isopreno são condensadas para formar uma molécula linear, precursora do colesterol, que é, então, organizada em uma estrutura cíclica.
Foi demonstrado que esqualeno, um hidrocarboneto poliisoprenoide, é o intermediário linear na biossíntese de colesterol pela observação de que animais alimentados com esqualeno marcado isotopicamente produziam colesterol marcado. O esqualeno pode ser dobrado de diversas maneiras, de modo a ciclizar e formar o núcleo esterol de quatro anéis. O padrão de dobramento proposto por Bloch e Robert B. Woodward provou estar certo.
O sumário dos principais estágios da biossíntese de colesterol, segundo Bloch, era
Acetato -> intermediário isoprenoide -> esqualeno -> produto ciclizado -> colesterol
Essa rota foi verificada experimentalmente e seus detalhes foram elaborados. Atualmente, sabe-se que isso é parte de uma rota ramificada, que produz vários outros isoprenoides essenciais, como ubiquinona (CoQ), dolicol, proteínas farnesiladas e geranilgeraniladas e isopentenil-adenosina (uma base modificada do tRNA). Será examinada com detalhes a porção dessa rota que sintetiza colesterol. Observe, entretanto, que mais de 25.000 isoprenoides (também chamados de terpenoides), na sua maioria originários de plantas, fungos e bactérias, foram isolados. Eles servem como constituintes de membranas (como o colesterol), hormônios (esteroides), feromônios, agentes defensivos, agentes fotoprotetores (p. ex., 13-carotenos) e pigmentos da visão (como os da retina), somente para citar algumas de suas muitas funções biológicas.
A - A HMG-CoA é um precursor-chave do colesterol
A acetil-CoA é convertida em unidades de isopreno por uma série de reações iniciadas pela farmação de hidroximetilglutaril-CoA (HMG-CoA), um composto que é também um intermediário na síntese de corpos cetônicos. A síntese de HMG-CoA requer a participação de duas enzimas: tiolase e HMG-CoA-sintase. Na mitocôndria, essas duas enzimas formam HMG-CoA para a síntese de corpos cetônicos, enquanto as isoenzimas citosólicas dessas duas proteínas geram a HMG-CoA que é usada na biossíntese de colesterol. Seus mecanismos catalíticos, contudo, são idênticos. A HMG-CoA é a precursora de dois intermediários isoprenoides, isopentenil-pirofosfato e dimetilalil-pirofosfato:-
A formação de isopentenil-pirofosfato envolve quatro reações:
1. O grupo tioéster da CoA na HMG-CoA é reduzido a álcool em uma redução de quatro elétrons dependente de NADPH, catalisada pela HMG-CoA-redutase, produzindo mevalonato.
2. O novo grupo OH é fosforilado pela mevalonato-5-fosfotransferase.
3. O grupo fosfato é convertido a pirofosfato pela fosfome-valonato-cinase.
4. A molécula sofre uma reação de descarboxilação, e o álcool resultante é desidratado pela pirofosfomevalonato-descarboxilase.
A HMG-CoA-redutase é a enzima limitante da velocidade na biossíntese de colesterol e é o principal sítio de regulação na rota. Essa enzima de 888 resíduos, ligada à membrana do retículo endoplasmático, é regulada, por mecanismos competitivos e alostéricos, fosforilação/desfosforilação e regulação de longo prazo. O próprio colesterol, por retroalimentação, é um importante regulador da enzima.


Resposta AULA
Mavelonato atua regulando via endógena, se come muito colesterol, ou seja exógeno, o Mavelonato age inibindo ainda mais a produção de colesterol endógeno. Estado bem alimentado libera insulina, e tendo bastante APT pois está bem alimentado, acaba construindo colesterol. O glucagon irá fazer o contrario pois irá priorizar o uso
R7 - Como a sinvastatina funciona?
As estatinas são agentes hipolipemiantes que exercem os seus efeitos através da inibição da HMG-CoA redutase, enzima fundamental na síntese do colesterol, levando a uma redução do colesterol tecidual e um conseqüente aumento na expressão dos receptores de LDL. Existem consideráveis diferenças entre as estatinas, no que tange às propriedades farmacocinéticas, bem como ao coeficiente de hidrofilicidade, via hepática de metabolização (especialmente, do citocromo P450 e isoenzimas), meia-vida plasmática e eficácia na redução lipídica. As estatinas também podem diferir na capacidade de interação com outras drogas que utilizam a mesma via de metabolização. Recentemente, muitos efeitos pleiotrópicos têm sido relatados com estas drogas, bem como propriedades antiinflamatórias, melhora na função endotelial e benefícios na hemostasia.
Algumas estatinas possuem uma grande seletividade de atuação, principalmente como decorrência de características como a lipossolubilidade. Neste aspecto, verifica-se que a pravastatina e a rosuvastatina são fármacos que podem ser considerados relativamente hidrossolúveis, quando comparados com as demais estatinas.
As estatinas atuam primariamente no fígado, onde um sistema especial de transporte permite sua incorporação ao tecido hepático para biotransformação, com ampla variação tanto no seu sítio metabólico, como formação de metabólitos ativos até sua eliminação pela bile. Alguns polimorfismos genéticos e a interação com alguns fármacos podem determinar dificuldade na sua captação, metabolização e eliminação.
O transporte para o tecido hepático parece influenciado pelos OATPs (Organic Anion Transporting Polypeptides), uma família de transportadores expressa em vários órgãos (Figura 6). No fígado o OATP-C constitui um membro específico desta superfamília e sua expressão foi confirmada por imunohistoquímica na membrana basolateral dos hepatócitos4. O OATP-C transporta várias substâncias, como ácidos biliares, conjugados glucuronidados, hormônios tireoidianos, peptídios, metotrexate e estatinas, incluindo a pravastatina, rosuvastatina e cerivastatina (comprovado) e atorvastatina (possível). Interações farmacológicas que reduzam a disponibilidade do OATP-C ou polimorfismos genéticos que diminuam sua expressão podem determinar redução da efetividade destas estatinas.
Após sua biotransformação, a eliminação das estatinas também pode ser influenciada por outro sistema transportador (glicoproteína-P), responsável pelo efluxo para a árvore biliar (gene MDR1- Multiple Drug Resistance), e novamente algumas interações entre fármacos ou polimorfismos também podem determinar acúmulo da vastatina no tecido hepático ou sua mais rápida eliminação. Assim, alguns inibidores de protease, digoxina, ciclosporina, entre outros, podem interferir na excreção hepática das estatinas.
Resposta AULA
Ezetiniba, atua inibindo a captação do colesterol pelo intestino, logo se o indivíduo consome pouco colesterol, mas produz muito, não adianta entrar com o medicamento. Nesse caso deve-se entrar com as estatinas para inibir a síntese endógena ou recaptação.

R8 - Quais as políticas publicas de prevenção de obesidade e hipertensão?
Programas com estímulo de exercícios físicos e alimentação saudável, controle glicêmico e de hipertensão. O SUS possui ainda uma RAS específica para hipertensão e diabetes.
SGLD1 faz galactose.
REFLEXÃO: Hoje a aula teve bastante assunto.
Vimos lipídios, suas características, funções, processo digestivo e de absorção, os tipos de colesterol, lipólise, via das pentoses, hipertensão.
A turma como sempre manda muito bem, porém sinto que o conhecimento é muito complexo ou seja, precisa ser relembrado em casa para fixar ainda mais.




Comentários